Nowe metody leczenia nerwiakowłókniakowatości: Co jest dostępne i jak uzyskać do nich dostęp w Wielkiej Brytanii?
Ostatnia aktualizacja: 11 marca 2025 r.
Możesz legalnie uzyskać dostęp do nowych leków, nawet jeśli nie zostały one zatwierdzone w Twoim kraju.
Dowiedz się jakNerwiakowłókniakowatość typu 1 (NF1) jest złożonym zaburzeniem genetycznym dotykającym około jedną na 3000 osób na całym świecie. W Wielkiej Brytanii żyje około 25 000 osób cierpiących na tę chorobę.
NF1 często prowadzi do rozwoju nerwiakowłókniaków splotowatych (pNF) - guzów, które mogą powodować ból, zniekształcenia i poważne powikłania. Do niedawna możliwości leczenia ograniczały się do operacji i leczenia objawowego.
W ostatnich latach nowe terapie celowane zapewniają lepszą kontrolę choroby i lepszą jakość życia. Pierwszą innowacją był Koselugo (selumetinib), pierwszy zatwierdzony przez FDA inhibitor MEK dla pNF związanych z NF1. W lutym 2025 r. FDA zatwierdziła również Gomekli (mirdametinib), co stanowi kolejny znaczący kamień milowy w leczeniu NF1.
Jeśli jesteś w Wielkiej Brytanii i zastanawiasz się, kiedy i jak możesz uzyskać dostęp do tych nowych metod leczenia NF1, oto, co musisz wiedzieć.
Jakie są najnowsze metody leczenia NF1?
Dwa najnowsze leki na NF1 zatwierdzone przez FDA są inhibitorami MEK. Oznacza to, że blokują one enzymy (MEK1/2) zaangażowane w sygnalizację wzrostu komórek. MEK1/2 są nadaktywne u pacjentów z NF1, co przyczynia się do wzrostu komórek nowotworowych. Blokując enzymy MEK, te nowe terapie neurofibromatozy mają na celu spowolnienie wzrostu komórek nowotworowych 1.
Gomekli (mirdametinib): Najnowszy lek na NF1 w 2025 r.
Gomekli (mirdametinib) jest inhibitorem MEK1/2, który celuje w szlak sygnałowy MAPK/ERK. Gomekli został zatwierdzony przez FDA w lutym 2025 r., a niektóre ze sposobów, w jakie różni się on od istniejących metod leczenia, są następujące:
- Podanie doustne. Gomekli może być przyjmowany z jedzeniem lub bez jedzenia i jest dostępny w postaci kapsułek, a także w postaci tabletek do sporządzania zawiesiny doustnej - jest to szczególnie odpowiednie dla dzieci, które nie mogą połknąć kapsułki.
- Zatwierdzony zarówno dla dorosłych, jak i dla dzieci. Gomekli jest wskazany do stosowania nie tylko u dorosłych pacjentów, ale także u dzieci w wieku 2 lat i starszych.
- Dobra skuteczność wykazana w badaniach klinicznych. W badaniu fazy 2 ReNeu, Gomekli wykazał pozytywne wyniki, przy czym 62% dorosłych i 52% dzieci osiągnęło >50% zmniejszenie wielkości guza 2.
Koselugo selumetinib): Inhibitor MEK dla pediatrycznych pacjentów z NF1
Koselugo było pierwszą terapią celowaną zatwierdzoną dla NF1 w 2020 roku. Do tej pory był zatwierdzony tylko dla dzieci w wieku 2 lat i starszych. Niektóre niedawno opublikowane wyniki badania fazy 3 KOMET sugerują, że może to być skuteczna opcja leczenia dla dorosłych z neurofibromatozą typu 1, a także 3. Jednak od marca 2025 r. nie jest on jeszcze zatwierdzony dla tej grupy docelowej.
Od 2021 r. selumetinib jest również zatwierdzony do stosowania w UE, a od 2022 r. również w Wielkiej Brytanii.
Oto szybkie porównanie Gomekli i Koselugo:
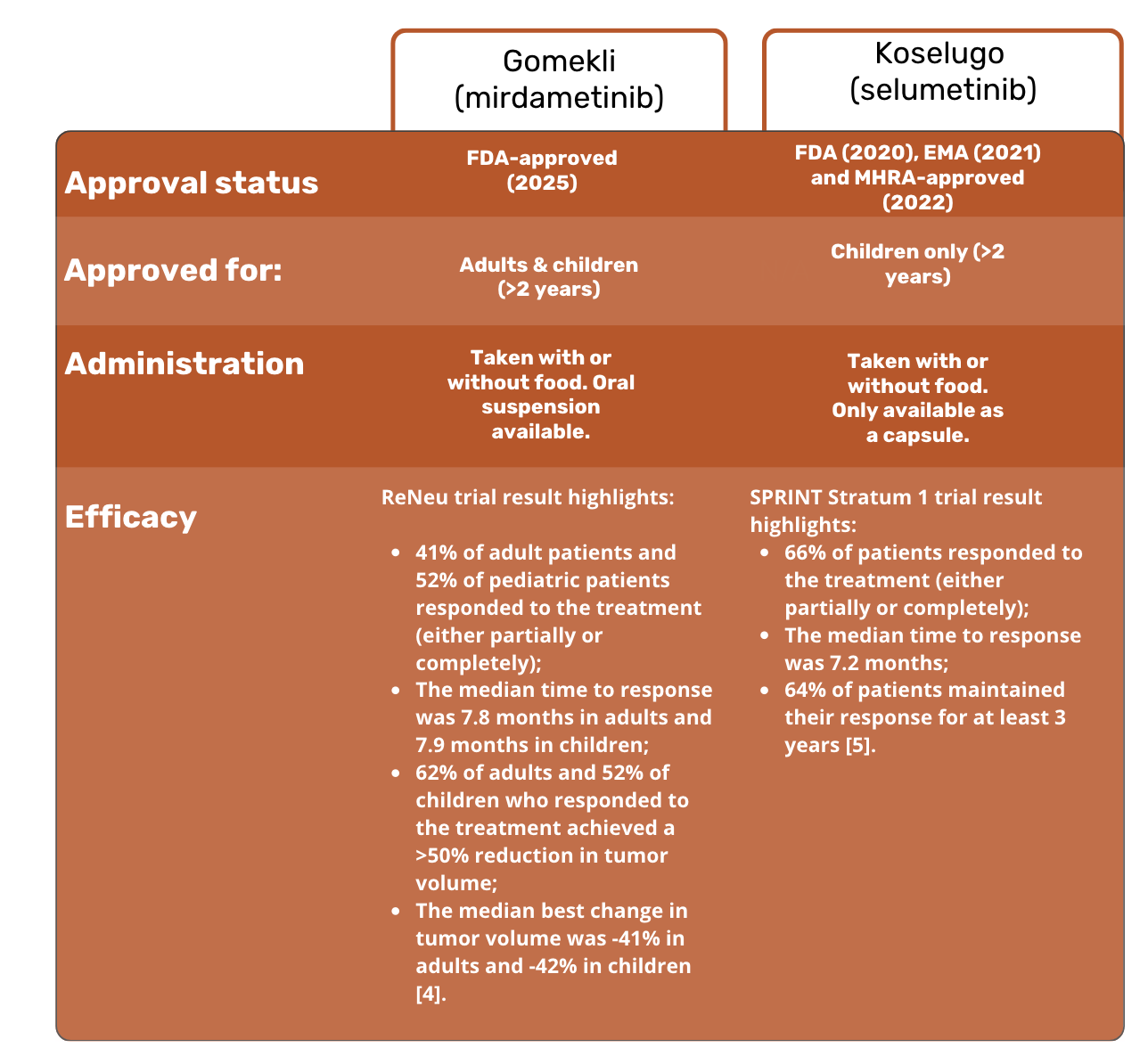

Czy Gomekli i Koselugo są dostępne w Wielkiej Brytanii?
Koselugo selumetinib) jest dostępny dla pacjentów w Wielkiej Brytanii i znajduje się w NHS 6.
Z drugiej strony Gomekli nie jest jeszcze dostępny w Wielkiej Brytanii, ani nie jest zatwierdzony ani dostępny w UE. Typowa procedura zatwierdzenia przez EMA trwa do 210 dni od złożenia wniosku, a w przypadku Gomekli żaden wniosek nie został jeszcze złożony. Oznacza to, że mogą minąć lata, zanim pacjenci z NF1 w UE i Wielkiej Brytanii uzyskają dostęp do tego leku.
Czy można kupić Gomekli w Wielkiej Brytanii, zanim zostanie zatwierdzony lokalnie?
Tak, możesz. Chociaż zatwierdzenia EMA i MHRA dla mirdametinibu nie są tuż za rogiem, pacjenci w Wielkiej Brytanii (i nie tylko) mają możliwość uzyskania dostępu do Gomekli przed jego oficjalną dostępnością. Jednym ze sposobów jest dołączenie do badania klinicznego. Innym jest uzyskanie Gomekli z zagranicy, na własny użytek.
Oto jak działa każda z opcji.
Dołącz do badania klinicznego
Aby uzyskać szybki dostęp do najnowszych metod leczenia nerwiakowłókniakowatości, można spróbować dołączyć do trwającego badania klinicznego. Aby to zrobić, musisz spełnić kryteria kwalifikacyjne. Potrzebne będzie również wsparcie lekarza prowadzącego. Warto pamiętać, że udział w badaniu nie gwarantuje, że zostaniesz przydzielony do grupy leczonej. Zamiast tego możesz otrzymać placebo.
Oto kilka dobrych miejsc, w których można zacząć szukać trwających badań klinicznych:
- ClinicalTrials.gov: Jest to baza danych zawierająca wszystkie badania kliniczne w USA. Jednak niektóre badania są również otwarte dla uczestników międzynarodowych. W chwili obecnej te badania mirdametinibu rekrutują pacjentów na całym świecie. Warto mieć je na oku.
- EUClinicaltrials.eu: Ta baza danych zawiera wszystkie badania kliniczne w Unii Europejskiej. Obecnie zawiera ograniczone informacje na temat badań rozpoczętych przed 31 stycznia 2022 roku. Informacje na temat tych badań można znaleźć w rejestrze badań klinicznych UE.
- myTomorrows: Organizacja ta wspiera pacjentów w znalezieniu opcji leczenia w badaniach klinicznych.
- Findmecure: Platforma umożliwiająca pacjentom znalezienie i dołączenie do badań klinicznych na całym świecie.
Pobierz Gomekli do użytku osobistego
Jeśli nie możesz wziąć udziału w badaniu klinicznym, możesz importować Gomekli z zagranicy na własny użytek. Jest to dozwolone na mocy rozporządzenia o imiennym imporcie pacjentów.
Jak to działa?
- Jeśli Gomekli zostanie zatwierdzony w innym kraju (np. USA) przed Wielką Brytanią, możesz go legalnie kupić i importować.
- Potrzebna będzie recepta od lekarza potwierdzająca, że lokalnie nie są dostępne odpowiednie alternatywy.
Potrzebujesz pomocy? Nasz zespół ekspertów ds. dostępu do leków w Everyone.org specjalizuje się w pomaganiu pacjentom w dostępie do nowych leków, zanim zostaną one zatwierdzone lokalnie. Skontaktuj się z nami, a z przyjemnością pomożemy Ci uzyskać dostęp do Gomekli w Wielkiej Brytanii.
Referencje:
- Koselugo | Europejska Agencja Leków (EMA). Europejska Agencja Leków, Dostęp 11 marca 2025 r.
- Mirdametinib uzyskuje priorytetowy przegląd FDA w neurofibromatozie typu 1 z PN. Targeted Oncology, 28 sierpnia 2024 r.
- Koselugo wykazało statystycznie istotny i klinicznie znaczący obiektywny odsetek odpowiedzi w porównaniu z placebo u dorosłych z neurofibromatozą typu 1 w globalnym badaniu fazy III KOMET. AstraZeneca, 12 listopada 2024 r.
- SpringWorks Therapeutics ogłasza prezentację danych na dorocznym spotkaniu Amerykańskiego Towarzystwa Onkologii Klinicznej (ASCO) w 2024 r. SpringWorks Therapeutics, 23 maja 2024 r.
- Koselugo® (selumetinib) | Skuteczność. Koselugo HCP, Dostęp 11 marca 2025 r.
- Selumetinib w leczeniu objawowych i nieoperacyjnych nerwiakowłókniaków splotowatych związanych z neurofibromatozą typu 1 u dzieci w wieku 3 lat i starszych. NICE, dostęp 11 marca 2025 r.