Adakveo vs Oxbryta: Zapoznanie się z alternatywami crizanlizumab
Ostatnia aktualizacja: 15 stycznia 2024 r.
Możesz legalnie uzyskać dostęp do nowych leków, nawet jeśli nie zostały one zatwierdzone w Twoim kraju.
Dowiedz się jak
Po cofnięciu zezwolenia na stosowanie Adakveo (crizanlizumab) w UE, wielu pacjentów i lekarzy musi znaleźć alternatywę dla Adakveo .
Jeśli odpowiedź na leczenie była dobra, nadal można uzyskać dostęp do strony Adakveo , nawet jeśli nie jest ona już zatwierdzona w UE. Jeśli jednak lekarz woli zmienić przebieg leczenia, dobrze jest zrozumieć, co to oznacza dla pacjenta.
W tym artykule przyjrzymy się jednej z możliwych alternatyw Adakveo , którą lekarz może chcieć omówić - Oxbryta (voxelotor). Tutaj znajdziesz krótki przegląd podobieństw i różnic między Adakveo i Oxbryta.
Adakveo vs Oxbryta: Do czego służą?
Zarówno Adakveo , jak i Oxbryta są lekami na receptę przeznaczonymi do leczenia choroby sierpowatokrwinkowej 1,2. Każdy z leków jest jednak ukierunkowany na inny aspekt choroby.
Adakveo ma na celu zmniejszenie częstości bolesnych kryzysów naczyniowo-okluzyjnych, podczas gdy Oxbryta jest stosowany w leczeniu niedokrwistości hemolitycznej u pacjentów z anemią sierpowatokrwinkową 1,2.
Dla jakiego wieku zatwierdzono Oxbryta w UE?
W przeciwieństwie do witryny Adakveo, która może być stosowana wyłącznie u pacjentów w wieku 16 lat i starszych, witryna Oxbryta jest również wskazana dla pacjentów pediatrycznych.
W USA lek Oxbryta może być przepisywany od 4. roku życia, podczas gdy w UE jego stosowanie u dzieci jest dozwolone dopiero od 12. roku życia 1,2.
Crizanlizumab vs Voxelotor: Jak działają?
Chociaż oba leki mają na celu zmniejszenie powikłań choroby sierpowatokrwinkowej, są one ukierunkowane na różne aspekty choroby.
Adakveo i ograniczenie bolesnych kryzysów
Adakveo ma na celu zmniejszenie częstotliwości bolesnych kryzysów, które występują, gdy zniekształcone komórki krwi utkną w naczyniach krwionośnych.
Substancja czynna leku, crizanlizumab, jest specyficznym rodzajem białka znanym jako przeciwciało monoklonalne. Białko to wiąże się z selektyną P, substancją znajdującą się na zewnętrznej warstwie komórek wyściełających naczynia krwionośne.
Selektyna P pomaga komórkom przylegać do naczyń krwionośnych i jest zaangażowana w blokowanie naczyń krwionośnych podczas bolesnych epizodów w chorobie sierpowatokrwinkowej. Łącząc się z selektyną P i hamując jej funkcję, Adakveo ma na celu zapobieganie tym bolesnym epizodom 3.
Oxbryta i zapobieganie anemii
OxbrytaZ drugiej strony ma na celu zapobieganie anemii związanej z chorobą sierpowatokrwinkową.
Aktywny składnik Oxbryta, voxelotor, zwiększa zdolność hemoglobiny do zatrzymywania tlenu i powstrzymuje ją przed tworzeniem sztywnych łańcuchów w naczyniach krwionośnych. Pomaga to czerwonym krwinkom zachować ich normalny kształt i elastyczność. Zmniejsza również tempo ich przedwczesnego niszczenia i wydłuża ich żywotność 4.
Jak wydajne są strony Adakveo i Oxbryta?
Skuteczność Adakveo (crizanlizumab) i Oxbryta (voxelotor) została zbadana w badaniach klinicznych.
-
Adakveo wyniki badań klinicznych
Adakveozatwierdzenie przez FDA, a także wstępne pozwolenie na dopuszczenie do obrotu w UE opierały się na wynikach badania klinicznego SUSTAIN. W badaniu porównano Adakveo (z lub bez hydroksymocznika) z placebo.
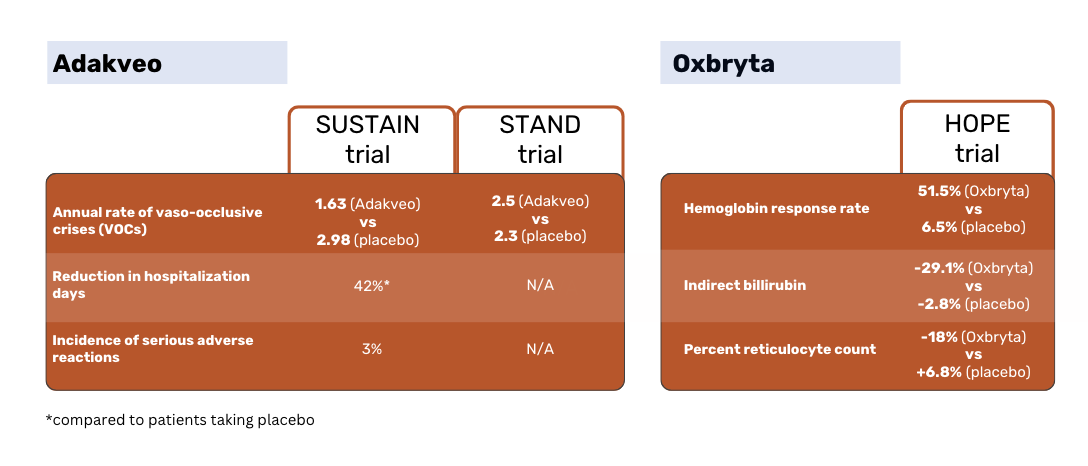
Zgodnie z wynikami badania SUSTAIN, pacjenci leczeni produktem Adakveo mieli statystycznie istotnie niższą medianę rocznego wskaźnika kryzysów naczyniowo-okluzyjnych (VOC) - 1,63 w porównaniu z 2,98 w przypadku pacjentów otrzymujących placebo. 36% pacjentów leczonych produktem Adakveo nie miało żadnych VOC w 52-tygodniowym okresie badania, w porównaniu do 17% pacjentów otrzymujących placebo 1.
Jakie były wyniki badania Adakveo STAND?
Globalne badanie fazy 3 STAND, w którym ponownie porównano Adakveo z placebo, nie wykazało statystycznie istotnej różnicy w częstości występowania VOC między grupami pacjentów. Pacjenci leczeni Adakveo mieli średnio 2,5 bolesnych kryzysów w ciągu roku leczenia - nie różniło się to znacząco od średnio 2,3 kryzysów zgłaszanych w grupie placebo 3.
Nieprzekonujące wyniki badania STAND stały się podstawą do wycofaniaAdakveo w UE.
-
Oxbryta wyniki badań klinicznych
W badaniu HOPE lek Oxbryta był testowany w porównaniu z placebo. Skuteczność oparto na wskaźnikach odpowiedzi hemoglobiny (Hb) zdefiniowanych jako wzrost Hb o >1 g/dL od wartości wyjściowej do tygodnia 24.
Oxbryta u pacjentów uzyskano odsetek odpowiedzi wynoszący 51,1% w porównaniu z 6,5% u pacjentów otrzymujących placebo. Bilirubina pośrednia zmniejszyła się o 29,1% u pacjentów z grupy Oxbryta w porównaniu ze spadkiem o 2,8% u pacjentów z grupy placebo. Procentowa liczba retikulocytów zmniejszyła się o 18% u pacjentów Oxbryta i wzrosła o 6,8& u pacjentów placebo 2.
Jak pokazują udostępnione dane, nie jest możliwe bezpośrednie porównanie obu leków, ponieważ w badaniach klinicznych zastosowano różne kryteria skuteczności. Ponieważ obie terapie podchodzą do choroby sierpowatokrwinkowej w inny sposób, jest prawdopodobne, że Oxbryta nie będzie bezpośrednim zamiennikiem Adakveo, ale raczej częścią nowego planu leczenia, który lekarz przygotuje dla pacjenta.

Adakveo vs Oxbryta: Bezpieczeństwo i skutki uboczne
Zgodnie z informacjami dotyczącymi przepisywania leków, są to najczęstsze działania niepożądane Adakveo i Oxbryta:
Adakveo skutki uboczne
- Mdłości
- Ból stawów
- Ból pleców
- Ból brzucha
- Fever1.
Podczas badania SUSTAIN u 3% pacjentów wystąpiły reakcje związane z infuzją, charakteryzujące się takimi objawami, jak ból głowy, dreszcze, wymioty, biegunka, duszność lub świszczący oddech 1.
Oxbryta skutki uboczne
- Bóle głowy
- Biegunka
- Ból brzucha
- Mdłości
- Rash
- Gorączka 2.
U mniej niż 1% pacjentów biorących udział w badaniach klinicznych wystąpiły poważne reakcje nadwrażliwości, w tym wysypka, łagodna duszność, łagodny obrzęk twarzy i eozynofilia (wzrost liczby białych krwinek)2.
Adakveo vs Oxbryta: Porównanie cen
Jeśli chodzi o ceny leków, które nie zostały jeszcze zatwierdzone lub nie są dostępne, należy je traktować wyłącznie jako orientacyjne. Ostateczna cena może się różnić w zależności od lokalizacji lub dostawcy.
Adakveo koszty roczne
Zalecana dawka dla Adakveo wynosi 5 mg/kg masy ciała co 4 tygodnie. Oznacza to 13 infuzji rocznie. Dla osoby ważącej 60 kg wymagałoby to 13 infuzji x 300 mg Adakveo lub 39 fiolek leku.
Przy cenie około 5 214 EUR za fiolkę 100 mg, roczny koszt leczenia Adakveo wynosi około 203 346 EUR 5.
Oxbryta koszty roczne
Zalecana dawka leku Oxbryta dla pacjentów o masie ciała powyżej 40 kg wynosi 1500 mg leku Oxbryta raz na dobę, co odpowiada 3 tabletkom x 500 mg każda.
Opakowanie 90 x 500 mg tabletek kosztuje około 40 365 EUR i wystarcza na jeden miesiąc, w oparciu o zalecane powyżej dawkowanie. W związku z tym roczny koszt leczenia Oxbryta wynosi 484 380 EUR 6.
Gdzie są zatwierdzone strony Adakveo i Oxbryta ?
Adakveo (crizanlizumab) jest obecnie zatwierdzony w kilku krajach, w tym w USA, Kanadzie i Australii 7,9,10. Jego warunkowe pozwolenie na dopuszczenie do obrotu w UE zostało cofnięte w maju 2023 r. 3.
Oxbryta (voxelotor) jest zatwierdzony w USA, UE i Kanadzie 4,8,9. Jednak w UE, Oxbryta nie jest jeszcze powszechnie dostępny na rynku, ponieważ czas między autoryzacją a wprowadzeniem na rynek może się znacznie różnić w zależności od kraju.
Czy Adakveo lub Oxbryta nie są (już) zatwierdzone lub dostępne w Twoim kraju? Jeśli Ty i Twój lekarz uważacie, że te terapie mogą przynieść Ci korzyści, skontaktuj się z naszym zespołem ekspertów ds. dostępu do leków. Możemy przedstawić spersonalizowaną ofertę cenową na pozyskanie leku dla Ciebie.
Referencje:
- NAJWAŻNIEJSZE INFORMACJE DOTYCZĄCE PRZEPISYWANIA. Novartis, dostęp 27 września 2023 r.
- NAJWAŻNIEJSZE INFORMACJE DOTYCZĄCE PRZEPISYWANIA LEKÓW. Oxbryta, dostęp 27 września 2023 r.
- Adakveo |Europejska Agencja Leków. Europejska Agencja Leków, dostęp 27 września 2023 r.
- Oxbryta |Europejska Agencja Leków. Europejska Agencja Leków, dostęp 27 września 2023 r.
- Kup Adakveo (crizanlizumab) Online. Everyone.org, Dostęp 27 września 2023 r.
- Kup Oxbryta (voxelotor) Online. Everyone.org, Dostęp 27 września 2023 r.
- Adakveo. Therapeutic Goods Administration (TGA), Dostęp 27 września 2023.
- FDA zatwierdza lek do leczenia niedokrwistości sierpowatokrwinkowej u dzieci. FDA, 17 grudnia 2021 r.
- Nowe leki zatwierdzone w 2019 roku - Meds Entry Watch. Canada.ca, 10 lutego 2021 r.
- FDA zatwierdza pierwszą terapię celowaną w leczeniu pacjentów z bolesnymi powikłaniami choroby sierpowatokrwinkowej. FDA, 15 listopada 2019 r.