Kiedy Vamorolone będzie dostępny w Europie i Wielkiej Brytanii? Pełna historia.
Ostatnia aktualizacja: 16 kwietnia 2024 r.

Możesz legalnie uzyskać dostęp do nowych leków, nawet jeśli nie zostały one zatwierdzone w Twoim kraju.
Dowiedz się jakKortykosteroidy od wielu lat stanowią standardową metodę leczenia pacjentów z dystrofią mięśniową Duchenne'a. Zwykle są one włączane do planu leczenia w wieku około 4 lub 5 lat, zanim wejdą w "fazę plateau" i doświadczą znacznej utraty siły 1. Niestety, długotrwałe stosowanie kortykosteroidów może wiązać się z różnymi skutkami ubocznymi, w tym zaburzeniami zachowania, przyrostem masy ciała, osteoporozą i innymi 2.
W tym kontekście niedawne zatwierdzenie przez FDA leku Agamree (vamorolone) jako "kortykosteroidu nowej fali" o mniejszej liczbie skutków ubocznych było bardzo potrzebnym przełomem w leczeniu Duchenne'a.
Podczas gdy vamorolone jest już spodziewany w aptekach w USA w pierwszym kwartale 2024 r., nie został on jeszcze zatwierdzony nigdzie indziej.
Kiedy vamorolone będzie dostępny w Europie i Wielkiej Brytanii? Oto wszystko, co musisz wiedzieć.
W jakim celu stosuje się vamorolone?
Agamree (vamorolone) jest wskazany do leczenia dzieci (4+) i dorosłych z dystrofią mięśniową Duchenne'a.
Agamree jest kortykosteroidem o działaniu dysocjacyjnym. Działa głównie poprzez łagodzenie stanów zapalnych w organizmie. Vamorolone działa podobnie do innych kortykosteroidów. Wiąże się jednak z komórkami w inny sposób i nie aktywuje pewnych reakcji organizmu, jak robią to inne sterydy.
Nie do końca wiadomo, w jaki sposób wamoloron działa na DMD (dystrofię mięśniową Duchenne'a). Wyniki badań klinicznych sugerują jednak, że pomaga on dzieciom cierpiącym na tę chorobę szybciej wstawać z pozycji leżącej i lepiej chodzić. Niektóre typowe działania niepożądane obejmują obrzęk, wymioty, przybieranie na wadze i drażliwość 3.
Czy vamorolone jest zatwierdzony przez EMA?
Od grudnia 2023 r. Agamree (vamorolone) jest zatwierdzony przez EMA do leczenia dystrofii mięśniowej Duchenne'a u dorosłych i dzieci w wieku powyżej 4 lat 3.
Kiedy vamorolone będzie dostępny w Europie?
Chociaż zatwierdzenie wamorolonu przez EMA to dobra wiadomość, nie oznacza to, że lek będzie dostępny od razu we wszystkich krajach europejskich. Zanim lek trafi do aptek, jego producent i lokalny organ ds. zdrowia w każdym państwie członkowskim muszą podjąć decyzje dotyczące lokalnego zatwierdzenia, cen i zakresu ubezpieczenia zdrowotnego. W rezultacie vamorolone będzie prawdopodobnie dostępny w różnym czasie w każdym kraju w Europie.
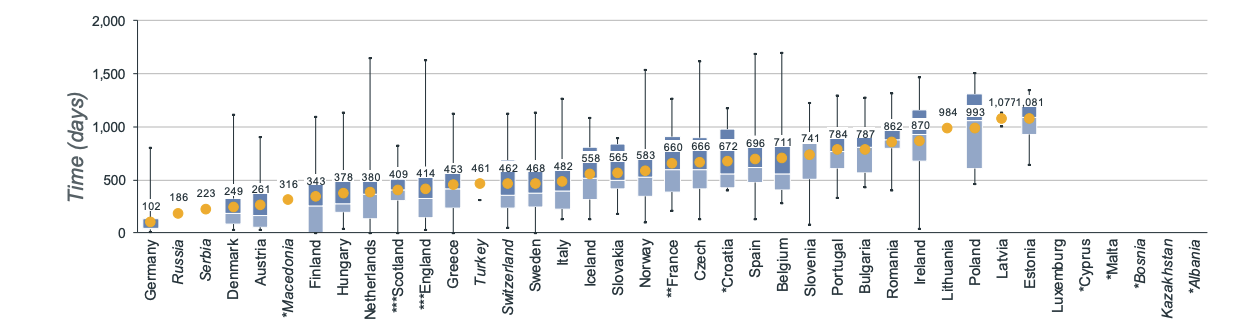
Nowe leki potrzebują średnio 511 dni od zatwierdzenia przez EMA, aby stać się dostępnymi w całej UE. Czas ten różni się znacznie w zależności od kraju. W przypadku leków sierocych, takich jak vamorolone, wynosi on od 102 dni w Niemczech do 1081 dni w Estonii5.
Kiedy vamorolone będzie dostępny w Wielkiej Brytanii?
Po zatwierdzeniu przez EMA, wamorolina została również zatwierdzona przez MHRA w Wielkiej Brytanii. Czyni to lek pierwszą terapią Duchenne'a zatwierdzoną łącznie w Wielkiej Brytanii, UE i USA.
Zanim wamorolon będzie dostępny w ramach NHS, NICE musi dokonać przeglądu i opublikować swoją decyzję w tej sprawie. Konsultacje są w toku, a projekt wytycznych spodziewany jest do końca kwietnia 2024 r .6 . W przypadku pozytywnej decyzji, Agamree powinien być dostępny dla pacjentów w ciągu 3 miesięcy od daty decyzji NICE.
Status zatwierdzenia Vamorolone w pozostałej części świata
Od kwietnia 2024 r. Agamree (vamorolone) nie jest zatwierdzony nigdzie indziej na świecie do leczenia dystrofii mięśniowej Duchenne'a 7.

Sposoby bezpiecznego dostępu do Agamree (vamorolone) przed jego zatwierdzeniem w Twoim kraju
Czy jesteś pacjentem z chorobą Duchenne'a spoza USA? Jeśli Twój lekarz uważa, że vamorolone może Ci pomóc, być może nie będziesz musiał czekać na lokalne zatwierdzenie lub dostępność Agamree. Zamiast tego, Twój lekarz i Ty możecie zbadać badania kliniczne wamorolonu. Możesz też kupić vamorolone od razu jako indywidualny pacjent.
Dołącz do badania klinicznego vamorolonu
Możesz dołączyć do badania klinicznego, aby otrzymać Agamree (vamorolone) lub inne niezatwierdzone leki. Znalezienie badania rekrutującego uczestników w danym kraju może być trudne, ale jest możliwe. Aby wziąć udział w badaniu, należy spełnić kryteria kwalifikacyjne. Potrzebne będzie również wsparcie lekarza prowadzącego.
Oto kilka dobrych miejsc, w których można rozpocząć poszukiwania trwających badań klinicznych vamorolonu:
- ClinicalTrials.gov: Jest to baza danych zawierająca wszystkie badania kliniczne w USA. Niektóre z badań są również otwarte dla uczestników międzynarodowych. Przykładem jest badanie kliniczne NCT05185622 z wamorolonem, które rekrutuje pacjentów w Kanadzie 8.
- EUClinicaltrials.eu: Ta baza danych zawiera wszystkie badania kliniczne w Unii Europejskiej. Obecnie zawiera ograniczone informacje na temat badań rozpoczętych przed 31 stycznia 2022 roku. Informacje na temat tych badań można znaleźć w rejestrze badań klinicznych UE.
- myTomorrows: Organizacja ta wspiera pacjentów w znalezieniu opcji leczenia w badaniach klinicznych.
Kup vamorolone na zasadzie indywidualnego imiennego pacjenta
W większości krajów pacjenci mogą legalnie kupować i importować leki, które mogą poprawić ich życie lub zaradzić stanom zagrażającym życiu. Jeśli chcesz uzyskać dostęp do wamorolonu, zanim będzie on dostępny w Twoim kraju, może to być opcja dla Ciebie i Twojego lekarza.
Rozporządzenie, które to umożliwia, jest znane jako rozporządzenie w sprawie importu danych osobowych pacjentów. Poszczególne kraje mogą różnić się pod względem konkretnych wymogów administracyjnych. Jednak we wszystkich przypadkach kryteria te muszą zostać spełnione:
-
Dany lek został zatwierdzony do obrotu w innym kraju i nie jest (jeszcze) zatwierdzony lub dostępny w kraju pacjenta;
-
Na lokalnym rynku nie ma alternatywy;
-
Lek jest przeznaczony do użytku osobistego;
-
Pacjent posiada receptę od lekarza prowadzącego;
-
Lekarz bierze odpowiedzialność za leczenie. Może to wymagać różnej dokumentacji w zależności od kraju.
Czy chcesz skorzystać z rozporządzenia w sprawie indywidualnego importu imiennego w celu uzyskania wamorolonu, zanim będzie on powszechnie dostępny w Europie, Wielkiej Brytanii lub innych krajach? Najpierw należy skonsultować się z lekarzem prowadzącym i uzyskać odpowiednią receptę.
Masz już receptę? Nasz zespół może pomóc w natychmiastowym zakupie vamorolone.
Referencje:
- Sterydy (kortykosteroidy). Parent Project Muscular Dystrophy, Dostęp 13 listopada 2023 r.
- Skutki uboczne długotrwałej terapii wysokimi dawkami sterydów, Dostęp 13 listopada 2023.
- Agamree: Dopuszczony do obrotu | Europejska Agencja Leków. Europejska Agencja Leków, 13 października 2023 r.
- Ubieganie się o pozwolenie na dopuszczenie do obrotu w UE produktów leczniczych stosowanych u ludzi. Europejska Agencja Leków, dostęp 13 listopada 2023 r.
- Badanie EFPIA Patients W.A.I.T. Indicator 2021. Efpia, dostęp 13 listopada 2023 r.
- Informacje o projekcie | Vamorolone w leczeniu dystrofii mięśniowej Duchenne'a [ID4024] | Wytyczne. NICE, dostęp 13 listopada 2023 r.
- AGAMREE® (vamorolone) - santhera. Santhera, Dostęp 13 listopada 2023 r.
- A Study to Assess Vamorolone in Boys Ages 2 to <4 Years and 7 to <18 Years With Duchenne Muscular Dystrophy (DMD). ClinicalTrials.gov, Accessed 13 November 2023.