Enhertu na raka płuc: Gdzie jest zatwierdzony i jak go zdobyć?
Ostatnia aktualizacja: 15 lipca 2024 r.
Możesz legalnie uzyskać dostęp do nowych leków, nawet jeśli nie zostały one zatwierdzone w Twoim kraju.
Dowiedz się jakEnhertu fam-trastuzumab deruxtecan-nxki) jest jednym z leków przeciwnowotworowych, które należy obserwować, od czasu jego pierwszego zatwierdzenia przez FDA w 2019 r. 1.
Ponieważ bezpieczeństwo i skuteczność Enhertu w raku jajnika i raku jelita grubego są nadal badane, lek jest już zatwierdzony dla kilku wskazań. W tym HER2-dodatni rak piersi, HER2-dodatni rak żołądka i rak piersi o niskim poziomie HER2. FDA zatwierdziła również Enhertu do stosowania w niedrobnokomórkowym raku płuca z mutacją HER2. CHMP w Europie wydał ostatnio pozytywną opinię w tej sprawie w ramach UE 2.
Jeśli jesteś pacjentem cierpiącym na raka płuc w Wielkiej Brytanii lub w innym miejscu poza USA i UE, prawdopodobnie zastanawiasz się, kiedy Enhertu będzie również dostępne dla Ciebie.
Oto wszystko, co należy wiedzieć o Enhertu w leczeniu raka płuc i czego mogą oczekiwać pacjenci w Wielkiej Brytanii i na całym świecie.
Jakie są wskazania do stosowania leku Enhertu w leczeniu raka płuc?
Jako terapia celowana, Enhertu jest przeznaczony wyłącznie do leczenia nowotworów z mutacją HER2. W związku z tym leczenie stosuje się u około 2% wszystkich pacjentów z NSCLC 3.
Enhertu jest wskazany w monoterapii u dorosłych pacjentów z zaawansowanym NSCLC, których guzy mają aktywującą mutację HER2 (ERBB2). Enhertu jest przeznaczony dla pacjentów, którzy otrzymali wcześniejszą terapię ogólnoustrojową i u których nowotwór rozprzestrzenił się na inne części ciała lub nie można go usunąć chirurgicznie 2.
Jaki jest wskaźnik skuteczności Enhertu w leczeniu raka płuc?
Trwające badanie fazy II DESTINY-Lung02 bada bezpieczeństwo i skuteczność Enhertu w leczeniu NSCLC z mutacją HER2. W badaniu porównywane są dwie dawki Enhertu (5,4 mg/kg i 6,4 mg/kg).
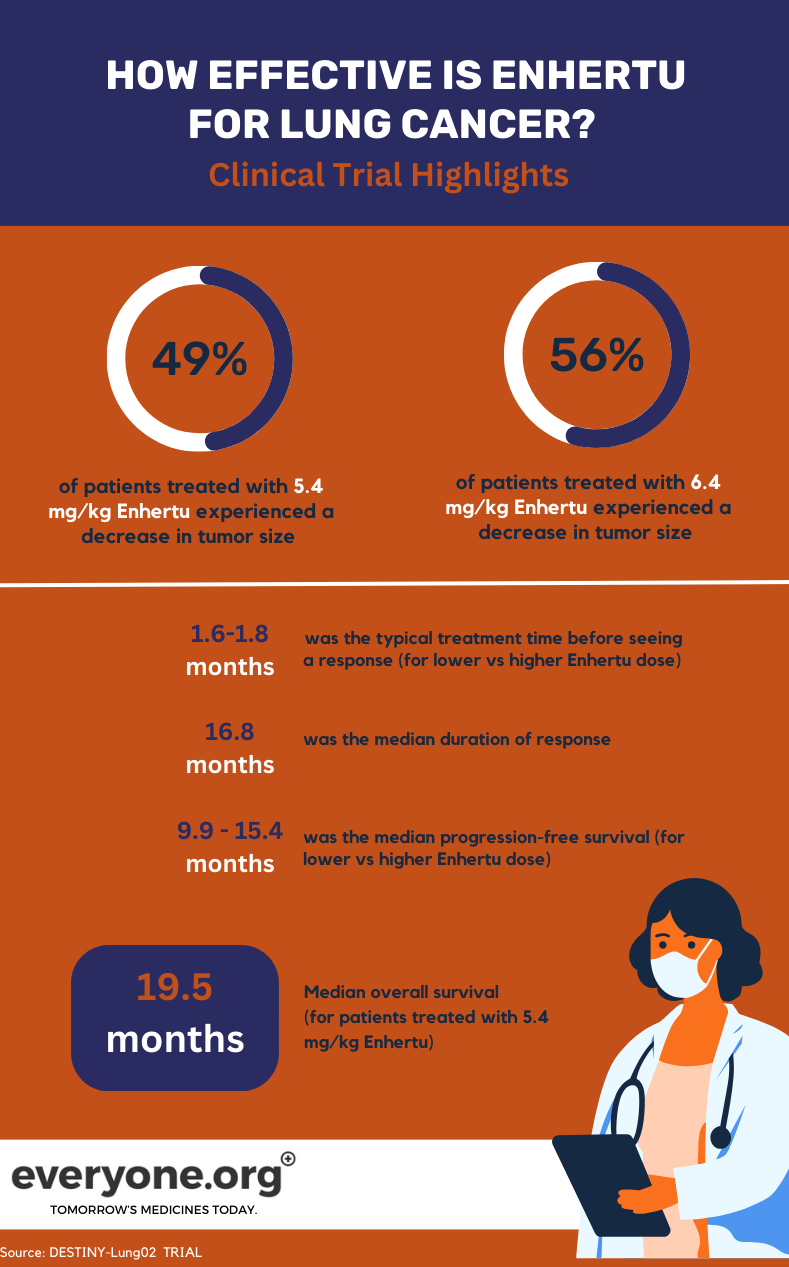
W przypadku pacjentów z rakiem płuca kluczowe wstępne wyniki badania DESTINY-Lung02 są następujące:
- Guzy zmniejszyły się u 49% pacjentów leczonych niższą dawką Enhertu i 56% pacjentów leczonych wyższą dawką.
- Guzy całkowicie zniknęły u 1% i 4% pacjentów w grupie otrzymującej odpowiednio niższą i wyższą dawkę.
- Mediana czasu trwania odpowiedzi wynosiła 16,8 miesiąca dla pacjentów w grupie niższej dawki Enhertu . W przypadku pacjentów z drugiej grupy, DoR został zgłoszony jako niemożliwy do oszacowania.
- Mediana czasu potrzebnego do zaobserwowania początkowej odpowiedzi na leczenie wynosiła 1,8 miesiąca i 1,6 miesiąca, odpowiednio w grupie niższych i wyższych dawek.
- Mediana przeżycia wolnego od progresji wynosiła 9,9 miesiąca przy dawce 5,4 mg/kg i 15,4 miesiąca przy dawce 6,4 mg/kg 4.
Jaka była mediana przeżycia pacjentów leczonych Enhertu ?
W przypadku pacjentów otrzymujących niższą dawkę Enhertu w badaniu klinicznym mediana całkowitego przeżycia (OS) wynosiła 19,5 miesiąca. OS został zgłoszony jako niemożliwy do oszacowania dla grupy otrzymującej wyższą dawkę 4.
Jakie są skutki uboczne Enhertu dla płuc?
U pacjentów leczonych produktem Enhertu zgłaszano ciężkie, zagrażające życiu lub śmiertelne przypadki śródmiąższowej choroby płuc (ILD). Pacjenci z umiarkowanymi zaburzeniami czynności nerek mogą być bardziej narażeni na ryzyko 6.
W badaniu DESTINY-Lung02 ILD odnotowano u 12,9% pacjentów w grupie niższych dawek i u 28% pacjentów w grupie wyższych dawek. Większość tych przypadków nie była ciężka. ILD stopnia 3 lub wyższego zgłoszono u 2% pacjentów w obu grupach pacjentów.
Profil bezpieczeństwa Enhertu w przypadku raka płuc jest podobny do jego skuteczności w innych wskazaniach. W oparciu o niższą częstość występowania działań niepożądanych (38,6% vs 58%), dawka 5,4 mg/kg jest uważana za optymalne leczenie pacjentów z NSCLC 4.

Gdzie zatwierdzono Enhertu w leczeniu raka płuc?
Obecnie Enhertu jest zatwierdzony w USA, UE, Izraelu i Japonii do leczenia dorosłych pacjentów z nieoperacyjnym lub przerzutowym NSCLC, których guzy mają aktywujące mutacje HER2 (ERBB2) 4.
Czy Enhertu jest zatwierdzony do stosowania w leczeniu raka płuc w Wielkiej Brytanii?
Od lipca 2024 r. jeszcze nie. W ostatecznym projekcie wytycznych opublikowanym przez NICE w marcu 2024 r. ogłoszono, że Enhertu nie będzie dostępny w NHS, dopóki nie będzie dostępna opłacalna cena. W międzyczasie Enhertu nie jest niestety dostępny w Wielkiej Brytanii w leczeniu raka płuc 7.
Czy mój lekarz może przepisać lek Enhertu na raka płuc, jeśli nie został on jeszcze zatwierdzony?
Krótka odpowiedź brzmi: tak.
Enhertu został już zatwierdzony w wielu krajach do leczenia NSCLC z mutacją HER2. Na tej podstawie lekarz ma prawo przepisać lek w tym wskazaniu, nawet jeśli nie został on jeszcze zatwierdzony w danym kraju.
Kiedy lekarz przepisuje lek w celu leczenia choroby, dla której nie został on (jeszcze) zatwierdzony, nazywa się to zastosowaniem poza wskazaniami. Recepta off-label może być trudna do zrealizowania w niektórych krajach, w zależności od lokalnych przepisów i dostępności. Zawsze jednak można ją zrealizować, korzystając z rozporządzenia w sprawie importu leków od określonego pacjenta.
Czy lekarz podjął decyzję o przepisaniu leku Enhertu w leczeniu raka płuc? Nasz zespół na stronieeveryone.org może pomóc w uzyskaniu dostępu do leku. Specjalizujemy się w pozyskiwaniu i dostarczaniu leków na receptę niezatwierdzonych lub niedostępnych w kraju pacjenta. Skontaktuj się z nami, abyśmy mogli Ci pomóc.
Referencje:
- Stewart, Judith. Enhertu (fam-trastuzumab deruxtecan-nxki) Historia zatwierdzeń FDA. Drugs.com, 15 sierpnia 2022 r.
- Enhertu. Europejska Agencja Leków, dostęp 06 listopada 2023.
- HER2 i rak płuca. American Lung Association, Dostęp 6 listopada 2023 r.
- Enhertu wykazał silną i trwałą odpowiedź guza w uprzednio leczonym zaawansowanym raku płuca z mutacją HER2 w badaniu fazy II DESTINY-Lung02. AstraZeneca, 11 września 2023 r.
- Informacje o projekcie | Trastuzumab deruxtecan w leczeniu nieresekcyjnego lub przerzutowego niepłaskonabłonkowego niedrobnokomórkowego raka płuca z mutacją HER2 po co najmniej 1 terapii [ID3934] | Wytyczne. NICE, dostęp 6 listopada 2023 r.
- USPI-DB-04 CDX Update FINAL. Daiichi Sankyo, dostęp 6 listopada 2023 r.
- Brytyjska NICE odrzuca Enhertu firmy Daiichi Sankyona raka piersi, Pharmaceutical Technology, dostęp 15 lipca 2024.