Czy Enhertu może leczyć raka jelita grubego? Najnowsze wyniki, terminy zatwierdzenia i nie tylko.
Ostatnia aktualizacja: 15 lipca 2024 r.
Możesz legalnie uzyskać dostęp do nowych leków, nawet jeśli nie zostały one zatwierdzone w Twoim kraju.
Dowiedz się jakOd czasu pierwszego zatwierdzenia przez FDA w 2019 r, Enhertu zyskał duże zainteresowanie w świecie onkologii. W 2023 r. Enhertu kontynuuje swoją imponującą trajektorię z dwoma dodatkowymi przełomowymi oznaczeniami FDA. Obecnie może pochwalić się łącznie siedmioma 1.
Jednym z najnowszych osiągnięć Enhertu jest jego zatwierdzenie jako leczenia antynowotworowego. Oznacza to, że można go teraz stosować u wszystkich pacjentów z nowotworami wykazującymi ekspresję HER2, w tym z nowotworem jelita grubego. Dla wszystkich pacjentów z rakiem jelita grubego jest to ważny kamień milowy. Jednocześnie rodzi to wiele pytań.
Oto wszystko, co musisz wiedzieć o Enhertu w przypadku raka jelita grubego.
Czy witryna Enhertu została zatwierdzona przez FDA do stosowania w leczeniu raka jelita grubego?
Tak. W kwietniu 2024 r. strona Enhertu została zatwierdzona do stosowania we wszystkich typach raka, w których występuje ekspresja HER2. Obejmuje to również raka jelita grubego.
Dla jakich typów nowotworów zatwierdzona jest witryna Enhertu ?
Enhertu jest obecnie zatwierdzony przez EMA w Europie do leczenia:
- HER2-dodatni rak piersi z przerzutami, którego nie można usunąć chirurgicznie;
- Rak piersi z przerzutami o niskim poziomie HER2, którego nie można usunąć chirurgicznie;
- HER2-dodatni zaawansowany rak żołądka lub rak połączenia żołądkowo-przełykowego 4.
W USA Enhertu jest dodatkowo zatwierdzony do leczenia:
- Przerzutowy niedrobnokomórkowy rak płuca z mutacją HER2 5.
- wszystkie guzy lite z ekspresją HER2.
Jaka jest skuteczność Enhertu w leczeniu raka jelita grubego?
Ponieważ Enhertu jest terapią celowaną, ma ona zastosowanie wyłącznie do nowotworów z ekspresją HER-2. Około 3-5% wszystkich nowotworów jelita grubego należy do tej kategorii 6.
Wyniki badań klinicznych
W czerwcu 2023 r. opublikowano ostateczne wyniki badania DESTINY-CRC01. To badanie fazy 2 koncentrowało się na ocenie skuteczności i bezpieczeństwa stosowania Enhertu u pacjentów z przerzutowym rakiem jelita grubego z ekspresją HER2. Pacjenci w badaniu mieli guzy, które uległy progresji po co najmniej 2 wcześniejszych rundach leczenia 7.
Kluczowe wyniki tego badania dla pacjentów z rakiem jelita grubego były następujące:
-
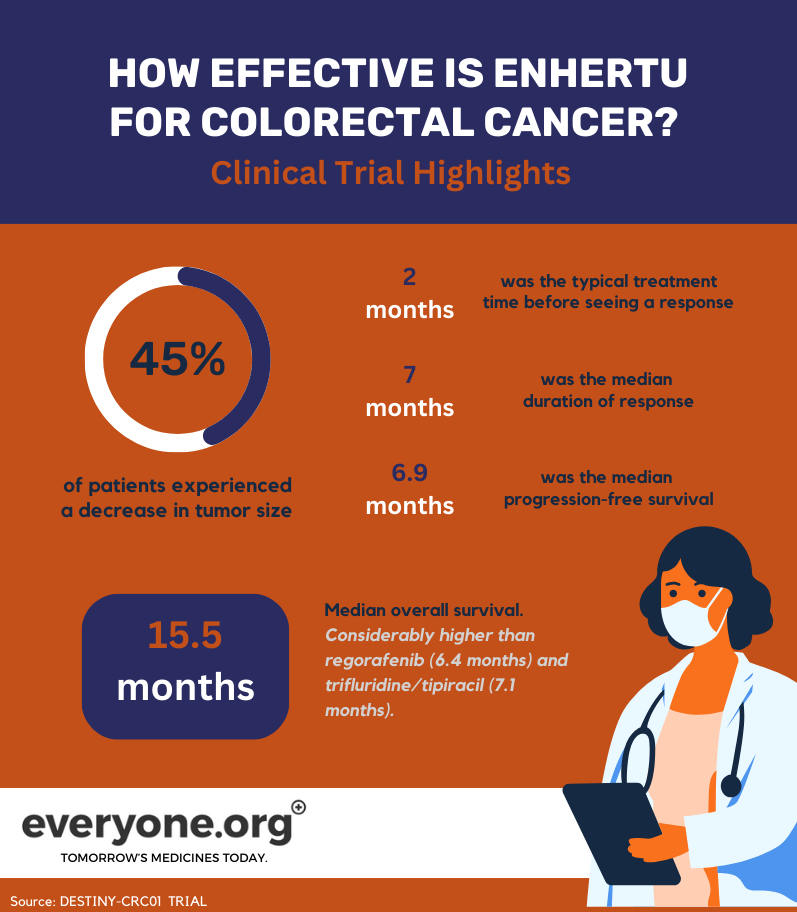
45,3% pacjentów leczonych za pomocą Enhertu doświadczyło częściowego obkurczenia guzów;
-
Odpowiedź na leczenie była zwykle widoczna po około 2 miesiącach od rozpoczęcia leczenia;
-
Mediana czasu trwania odpowiedzi wynosiła 7 miesięcy;
-
Mediana przeżycia wolnego od progresji wynosiła 6,9 miesiąca;
-
Mediana całkowitego przeżycia wyniosła 15,5 miesiąca. Wynik ten znacznie przekracza obecny standard opieki. Na przykład, regorafenib i trifluridine/tipiracil są powszechnymi terapiami trzeciego rzutu. Przeżycie całkowite w tych terapiach wynosi odpowiednio 6,4 miesiąca i 7,1 miesiąca7.
Inne badanie, o nazwie DESTINY-CTC02, bada Enhertu u pacjentów z rakiem jelita grubego. Badanie jest nadal w toku, ale jego wstępne wyniki są zgodne z wynikami badania DESTINY-CTC01 10.

Jak bezpieczne jest Enhertu w przypadku raka jelita grubego?
Pod względem bezpieczeństwa są to główne wyniki badania DESTINY-CRC01:
-
U każdego pacjenta wystąpiły skutki uboczne leczenia. Najczęstszymi skutkami ubocznymi były problemy z żołądkiem i krwią.
-
Poważne działania niepożądane wystąpiły u 37,7% pacjentów. Najczęstszymi poważnymi działaniami niepożądanymi były niska liczba neutrofili (22,1%) i niedokrwistość (14%) 7.
-
Działanie niepożądane zwane śródmiąższową chorobą płuc (ILD) było związane z odstawieniem leku i zaobserwowano je u 7% pacjentów.
-
Zgłoszono 3 zgony związane z lekami, z których wszystkie były związane ze śródmiąższową chorobą płuc.
Co to oznacza?
Enhertunie mogą być bezpośrednio porównywane między różnymi grupami pacjentów. Jednak, aby pomóc Ci umieścić rzeczy w kontekście, oto podsumowanie wyników bezpieczeństwa Enhertu w różnych typach nowotworów. W tym nowotworów, dla których zatwierdzono Enhertu :
-
ILD wystąpiła u 12% badanych pacjentów, ze skutkiem śmiertelnym w 1,5% przypadków;
-
Obniżona liczba neutrofili wystąpiła u 34,6% badanych pacjentów;
-
Niedokrwistość wystąpiła u 34-43% badanych pacjentów (w zależności od dawki leku) 8.
Biorąc to pod uwagę, profil bezpieczeństwa Enhertu w przypadku raka jelita grubego jest podobny do jego profilu w przypadku innych zatwierdzonych nowotworów.
Kiedy witryna Enhertu zostanie zatwierdzona do stosowania w leczeniu raka jelita grubego?
Enhertu jest już zatwierdzony przez FDA w leczeniu HER2-dodatniego raka jelita grubego - wskazanie, które wchodzi w zakres ostatniego zatwierdzenia przez FDA Enhertu.
Jednak to najnowsze zatwierdzenie jest faktem tylko w USA. Co to oznacza dla pacjentów z rakiem jelita grubego w innych krajach? Jaką rolę może odegrać Enhertu w leczeniu CRC?
Czy mój lekarz może przepisać Enhertu na raka jelita grubego?
Krótka odpowiedź brzmi: tak.
Enhertu jest już zatwierdzony przez FDA do leczenia HER2-dodatniego raka jelita grubego. Nawet jeśli mieszkasz w innym kraju, Twój lekarz i tak ma prawo przepisać lek w tym wskazaniu. Może to zrobić na podstawie ostatecznych wyników badania DESTINY-CRC01 lub wstępnych wyników badania DESTINY-CRC02 oraz specyfiki Twojego przypadku.
Jeśli lekarz przepisze ci lek na chorobę, dla której nie jest on lokalnie zatwierdzony, jest to stosowanie poza wskazaniami. W niektórych krajach realizacja recepty na lek off-label może być trudna ze względu na lokalne przepisy i dostępność. Zawsze jednak można ją zrealizować, korzystając z rozporządzenia w sprawie importu leków przez Nazwanego Pacjenta.
Czy lekarz podjął decyzję o przepisaniu leku Enhertu w leczeniu raka jelita grubego? Nasz zespół pod adresem www.everyone.org może pomóc w uzyskaniu dostępu do leku. Specjalizujemy się w pozyskiwaniu i dostarczaniu leków na receptę niezatwierdzonych lub niedostępnych w kraju pacjenta. Skontaktuj się z nami, abyśmy mogli Ci pomóc.
Referencje:
- Barrie, Robert. Enhertu zdobywa dwa oznaczenia przełomowej terapii FDA. Technologia farmaceutyczna, 31 sierpnia 2023 r.
- FDA przyznaje przełomowe oznaczenia terapeutyczne dla trastuzumabu Deruxtecan dla guzów litych HER2+, w tym mCRC. OncLive, 31 sierpnia 2023 r.
- Przełomowa terapia. FDA, 4 stycznia 2018 r.
- Enhertu |Europejska Agencja Leków. Europejska Agencja Leków, dostęp 30 października 2023 r.
- Stewart, Judith. Enhertu (fam-trastuzumab deruxtecan-nxki) Historia zatwierdzeń FDA. Drugs.com, 15 sierpnia 2022 r.
- Biomarker HER2 w raku okrężnicy. Know Your Biomarker, 24 maja 2023 r.
- Końcowe wyniki badania DESTINY-CRC01 badającego trastuzumab deruxtecan u pacjentów z przerzutowym rakiem jelita grubego z ekspresją HER2. Nature Communications, dostęp 30 października 2023 r.
- Enhertu, INN-trastuzumab deruxtecan. Europejska Agencja Leków , Dostęp 30 października 2023.
- Trastuzumab Deruxtecan u uczestników z zaawansowanym lub przerzutowym rakiem jelita grubego z nadekspresją HER2 (DESTINY-CRC02). ClinicalTrials.gov, dostęp 30 października 2023 r.
- Trastuzumab deruxtecan (T-DXd) u pacjentów z przerzutowym rakiem jelita grubego (mCRC) z nadekspresją/amplifikacją HER2 (HER2+): Podstawowe wyniki wieloośrodkowego, randomizowanego badania fazy 2 DESTINY-CRC02. Journal of Clinical Oncology, dostęp 30 października 2023 r.